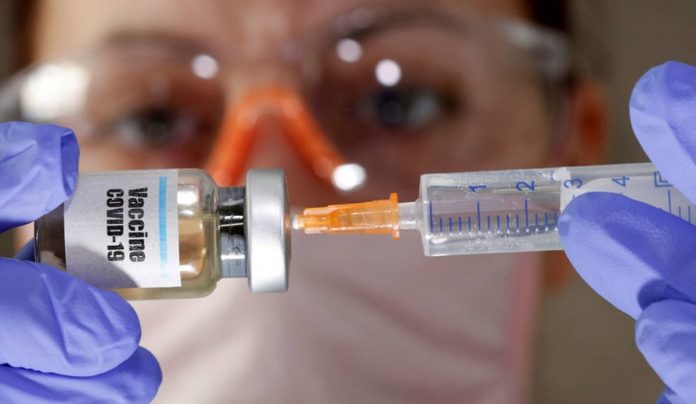
Pfizer (EEUU) y BioNTech (Alemania) dijeron que comenzaron a administrar dosis de sus vacunas experimentales del coronavirus para pruebas iniciales en humanos en Estados Unidos. Con información de Reuters.
Estudio de EEUU revela el fármaco más efectivo contra el coronavirus
Las farmacéuticas señalaron que si la vacuna demuestra ser segura y efectiva en los ensayos, podría estar lista para una amplia distribución en EEUU para fin de año, lo que reduciría varios años el plazo de desarrollo de la vacuna.
La vacuna, que utiliza la tecnología de ARN mensajero (ARNm), tiene el potencial de estar entre las primeras vacunas contra el virus que ha infectado a más de 1 millón de personas en Estados Unidos y ha matado a unas sesenta y ocho mil.
Actualmente no hay tratamientos o vacunas aprobados para el nuevo coronavirus, aunque algunos medicamentos se están utilizando en pacientes bajo una autorización de uso de emergencia.
El estudio de Estados Unidos es parte de un programa global más amplio que ya está en marcha en Alemania, donde se encuentra BioNTech. La dosificación allí comenzó el mes pasado.
Empresas de todo el mundo se unen para combatir el coronavirus
La compañía de biotecnología Moderna Inc (UK), está utilizando tecnología similar para el desarrollo de su vacuna junto con el gobierno de Estados Unidos. La prueba de fase I de ese candidato a vacuna también ha comenzado, con ensayos de etapa intermedia planificados en el trimestre actual.
Pfizer dijo la semana pasada que espera recibir autorización de emergencia de la Administración de Drogas y Alimentos de Estados Unidos a principios de octubre, y que podría distribuir hasta 20 millones de dosis para fines de 2020, con miras a producir cientos de millones de dosis el próximo año.
«Incluso pasar de unos pocos millones a 20 millones le permitirá proteger los epicentros del virus y luego expulsarlo de nuestra sociedad a medida que aumentamos a cientos de millones», dijo el jefe de investigación de Pfizer.
El uso de la tecnología de ARNm sintético puede permitir que la vacuna se desarrolle y fabrique más rápidamente que las vacunas tradicionales, dijeron las compañías.
Pfizer dijo la semana pasada que espera que los datos de seguridad sobre la vacuna estén disponibles a fines de mayo.
Inicialmente, el ensayo tendrá como objetivo probar diferentes regímenes de dosificación de cuatro posibles candidatos a vacunas en alrededor de 360 voluntarios sanos divididos en una cohorte más joven y un grupo de personas mayores.
El estudio se ampliará a más sujetos después de que los investigadores determinen qué compuestos y regímenes de dosificación son más efectivos, afirmó la directora del Centro de Desarrollo de Vacunas y Salud Global de la Universidad de Maryland.
Ya se han administrado dosis a algunos voluntarios en la Escuela de Medicina Grossman de la NYU y en la Escuela de Medicina de la Universidad de Maryland.
Empresas venezolanas con impresoras 3D se unen a la lucha contra el coronavirus
Pfizer planea expandir la prueba a sitios en todo Estados Unidos a principios de julio y, en última instancia, puede inscribir a más de ocho mil participantes, dijo una portavoz de la compañía.
Si tiene éxito, el ensayo clínico en EEUU sería una de las progresiones más rápidas de una vacuna desde los estudios iniciales hasta la aprobación regulatoria, lo que comprime un proceso de desarrollo que a menudo lleva de una década a poco más de 9 meses.
«Esto es el equivalente a hacer las fases uno, dos y tres de un ensayo clínico típico, pero todo comprimido en el marco de tiempo de mayo a octubre».
BioNTech está produciendo la vacuna para los ensayos en sus instalaciones de fabricación europeas. Pfizer está invirtiendo en el desarrollo de su propia capacidad de fabricación para la vacuna, y está preparando sitios en Massachusetts, Michigan, Missouri y Bélgica para comenzar a producirla.
Ambas compañías comercializarán conjuntamente la vacuna, si se aprueba.